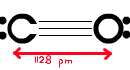
一酸化炭素(CO)は可燃性の無色・無臭の気体である。融点は−205 °C、沸点は−192 °Cである。
概要
化学式はCOと表す。いくつかの共鳴構造をとる。無色・無臭の気体である(常温・常圧)
錯体化学では配位子として重要であり有機化学でもカルボニル基(>C=O)の導入において有用な物質である。
一酸化炭素中毒
酸素の約250倍も赤血球中のヘモグロビンと結合しやすいため、体内の酸素循環を阻止することとなる。
| 各気体の分子量 | |
| 空気(平均) | 28.966 |
| 一酸化炭素 | 28.010 |
| 二酸化炭素 | 44.01 |
症状に気づきにくいため、気づかぬうちに昏睡状態となり最悪の場合は死に至るおそれがある。
また、火災のときにしゃがんで移動するといわれたことがあると思うが、それは一酸化炭素は空気より僅かに軽いため空気より上部にたまりやすい一酸化炭素を吸わないためである。各気体の重さ(分子量)を右に示す。
一酸化炭素に一時間さらされた場合、500ppmで症状が現れはじめ、1000ppmでは顕著な症状、1500ppmで死に至るとされている。
発生方法
HCOOH(メタン酸(ギ酸))をH2SO4(濃硫酸)で脱水することによって発生させることが可能。
水上置換で集めることが可能であるが、前述の通り有毒性があるので扱いには注意すること。
工業的には空気を絶って高温に加熱した炭コークスに水を反応させることによって合成している。(意外に一酸化炭素の用途は広い。)
また、希望を失った一部の人は練炭の不完全燃焼で合成しているが、収率が低いため工業的には使われない。
一酸化炭素の詳しい構造
一酸化炭素は共鳴をするので共鳴安定化エネルギーを得ている。最も寄与の大きい(安定な)極限構造式はCとOが3重結合をしている構造である(上の画像の構造)。ちなみに、共鳴とはある原子の電子は通常の自分の原子まわりで動きが束縛されている状態だが、共鳴できる分子というのは、分子の全体あるいは一部に電子が広がって安定化していることをいう。
有機合成における有用性
①ハロゲン化アリールにパラジウムなどの金属触媒と求核剤を加えたクロスカップリングにおいて、一酸化炭素を共存させるとカルボニル基が導入される。
Ar−Br+ ROH→ Ar−C(=O)−OR (エステルの合成);パラジウム触媒
②Gattermann-Kochホルミル化反応でも用いられる。Gattermann-Kochホルミル化反応はベンゼンからベンゼン誘導体であるベンズアルデヒドを直接合成する手法である。これはベンゼンの記事のFriedel-Craftsアシル化に詳しい。
関連項目
- 6
- 0pt